Element nedir?
Kimyasal çözümlemeyle ayrıştırılamayan veya bireşim yoluyla elde edilemeyen maddeye element denir.
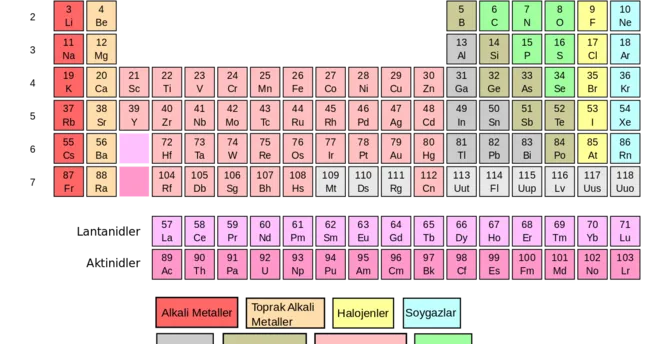
Çok eskiden beri kimyacilar, elementleri siniflandirmayi düsünmüslerdi. Böyle bir siniflandirmada elementlerin özellikleri, belirli bir düzen içinde degisirse, kimyacilarin isi epeyce kolaylasacakti. Geçen yüzyilin ortalarinda, simdi bilinen elementlerin yarisindan biraz fazlasi biliniyordu. Bilinen elementleri, özelliklerine göre siniflandirmak için o zamanki kimyacilar, degisik fikirler ileri sürmüslerdir.
Bugünkü anlama yakin periyodik sistem, 1869 yilinda Rus kimyacisi Dimitri Mendeleev tarafinda yapilmistir. 1877 yilinda Alman bilgini Lothar Meyer de Mendeleev' den habersiz olarak bir periyodik cetvel yapmistir. Bu iki cetvel hemen hemen birbirinin aynidir. Meyer; elementleri, cetvelinde fiziksel özelliklerine göre siralamis, Mendeleev ise elementlerin atom kütlelerini dikkate alarak artan atom kütlelerine göre cetvelinde siralamistir. Bu siralamada birbirini izleyen elementlerin degerliklerinin ve öteki özelliklerinin, belirli sayida elementten sonra tekrarladigini, yani bu özelliklerin periyodik oldugunu görmüstür.
Mendeleev; hidrojen elementini, özellikleri o zaman bilinen elementlerin özelliklerine benzedigi için ayri birakarak ondan sonra gelen elementleri (Li, Be, B, C, N, O, ve Fu) bir satir üzerinde (periyotta) atom kütlelerine göre siraladi. Böylece, bu elementlerin özelliklerinin ve degerliklerinin adim adim degistigini gördü. O gün için bilinen ve atom kütlesine göre flüordan sonra gelen element sodyum idi. Sodyumun özellikleri, ondan öncekilere degil, lityumun özelliklerine benzediginden, sodyumu ikinci satirin(periyodun) basina, lityumun altina getirmesi gerekmis ve bu suretle de yeni bir periyot baslamistir. Bu periyotta sodyumdan sonra, birinci periyottaki elementlere adim adim benzeyen Mg, Al, Si, P, S ve Cl gelir. Bunlardan sonra atom kütlesine göre sirasi gelen element potasyumdur
Bunun özellikleri : sodyumuna benzedigi için sodyumun altinda potasyum yer alacak sekilde, potasyum ile yeni bir periyot baslar. Potasyum ile baslayan bu yeni periyotta atom kütlesine göre sirasi gelen element kalsiyumdur. Kalsiyumun özellikleri magnezyumunkine benzedigi için onun altina yeni ikinci sütuna yerlestirilir. Kalsiyumdan sonra o zaman bilinen element titandi. Ancak titani, özellikleri bakimindan alüminyumun altinda göstermeye imkan olmadigini gören Mendeleev, üstün bir önseziyle, kalsiyum ile titan arasinda bir elementin bulunmasi gerektigini söylemistir. Bu nedenledir ki Mendeleev, atom kütleleri sirasina göre kurdugu gruplarda, özellik bakimindan benzeyen element yoksa, yerini bos birakmistir. Bunun sonucu olarak Mendeleev' in periyodik cetvelinde bazi bosluklar meydana gelmistir. Mendeleev, bu bosluklari açiklamasini bilmis, o gün için bilinmeyen ve periyodik cetvelde 32 numarali yeri almasi gereken elementin özelliklerinin ne olacagini tahmin etmistir. Ayrica, Mendeleev' in sisteminde bos kalan yarlarda bilinmeyen elementlerdir.







